Modelo Atómico De Böhr. Linea de tiempo con los principales modelos átomicos.

Resumen: características principales. El modelo atómico de Bohr, propuesto por Niels Bohr en 1913, fue una teoría que revolucionó nuestra comprensión de la estructura atómica. Sus puntos clave incluyen: Niveles de energía cuantizados: Los electrones en un átomo ocupan órbitas discretas llamadas "niveles de energía".
Modelo Atómico de Bohr » Modelos Atomicos

El modelo atómico de Bohr es una teoría científica desarrollada por el físico danés Niels Bohr en 1913. Este modelo describe la estructura del átomo y cómo los electrones se comportan en su interior. En el modelo de Bohr, los electrones giran alrededor del núcleo del átomo en órbitas circulares definidas y estables.
El Para Qué Sirve Conocer El Modelo Atómico De Bohr Diario La fisica y quimica
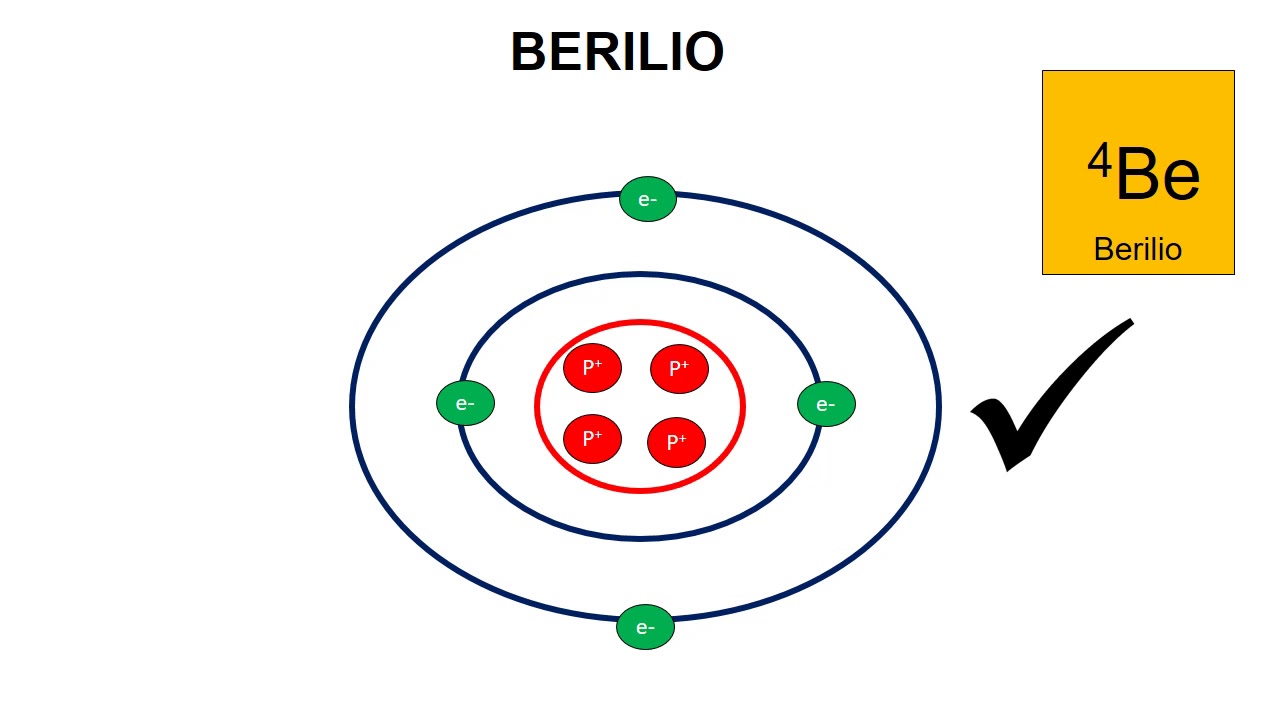
Contenido. Características del modelo atómico de Bohr. Postulados del modelo atómico de Bohr. Primer postulado: Los electrones se mueven a una cierta distancia del núcleo. Segundo postulado: Los electrones siguen una trayectoria circular. Tercer postulado: Los electrones emiten luz cuando cambian de nivel. ¿De dónde surgió el modelo.
PPT EL ÁTOMO DE BOHR historia del átomo PowerPoint Presentation ID5439337
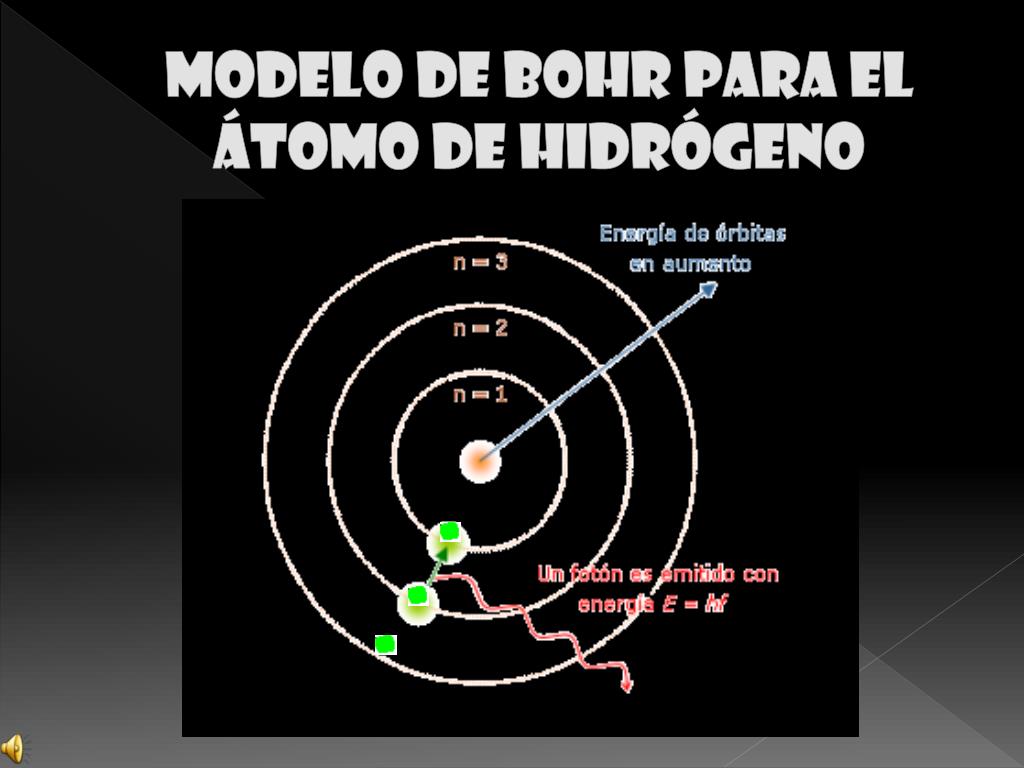
El modelo de Bohr propone que los electrones se mueven en órbitas circulares alrededor del núcleo del átomo, pero con niveles de energía cuantizados. Esto significa que no pueden tener cualquier cantidad de energía, sino que están restringidos a ciertos valores específicos. Cuando un electrón salta de un nivel de energía a otro, emite.
Resultado de imagen de modelo atomico de bohr Modelos atomicos, Modelo atómico de bohr, Átomo

Niels Bohr fue un físico danés que en 1913 propuso un nuevo modelo para explicar la estructura del átomo y su comportamiento a través de la estabilidad de los electrones. Por este decisivo aporte al conocimiento recibió el Premio Nobel de Física en 1922. El modelo planteado por Bohr funcionó para comprender el funcionamiento de ciertos.
Historia Del Átomo Modelo Atómico De Bohr Modelo atomico de diversos tipos

Bohr y su modelo atómico. En el campo de la física, el modelo atómico propuesto por Niels Bohr en 1913 jugó un papel fundamental en la comprensión de la estructura y comportamiento de los átomos.
Explicando El Modelo Atómico De Bohr Discutiendo Modelos
+Corrigió+los+errores+de+Rutherford..jpg?ssl=1)
El modelo atómico de Bohr es la concepción del físico danés Niels Bohr (1885-1962) acerca de la estructura del átomo, publicada en 1913. En el átomo de Bohr, los electrones alrededor del núcleo ocupan únicamente ciertas órbitas permitidas, gracias a una restricción llamada cuantización.. Para Bohr, la imagen del átomo como un sistema solar en miniatura, con los electrones orbitando.
Modelo atómico de Bohr ️ ¿Qué es? ️ ¿En que consiste?
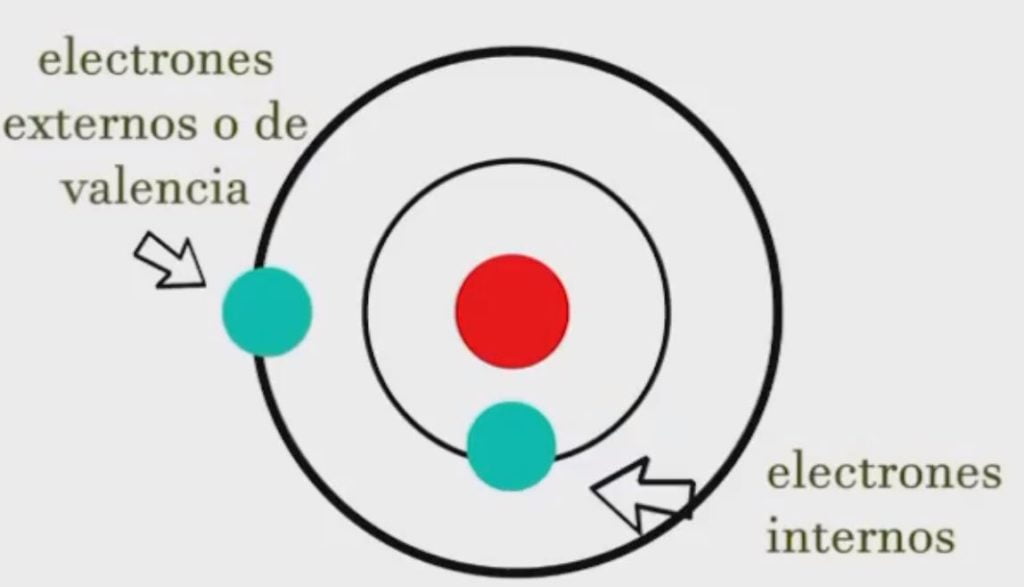
que es idéntica a la ecuación de Rydberg en la que R ∞ = k h c. R ∞ = k h c. Cuando Bohr calculó su valor teórico para la constante de Rydberg, R ∞, R ∞, y lo comparó con el valor aceptado experimentalmente, obtuvo una excelente concordancia. Dado que la constante de Rydberg era una de las constantes que se medían con mayor precisión en aquella época, este nivel de concordancia.
PPT MODELO ATÓMICO DE BOHR PowerPoint Presentation, free download ID1110283

Puntos más importantes. El modelo del hidrógeno de Bohr está basado en la suposición clásica de que los electrones viajan en capas específicas, u órbitas, alrededor del núcleo. Bohr explicó el espectro del hidrógeno en términos de electrones que absorben y emiten fotones para cambiar niveles de energía, en donde está la energía.
Modelo atómico de Bohr explicacion sencilla YouTube
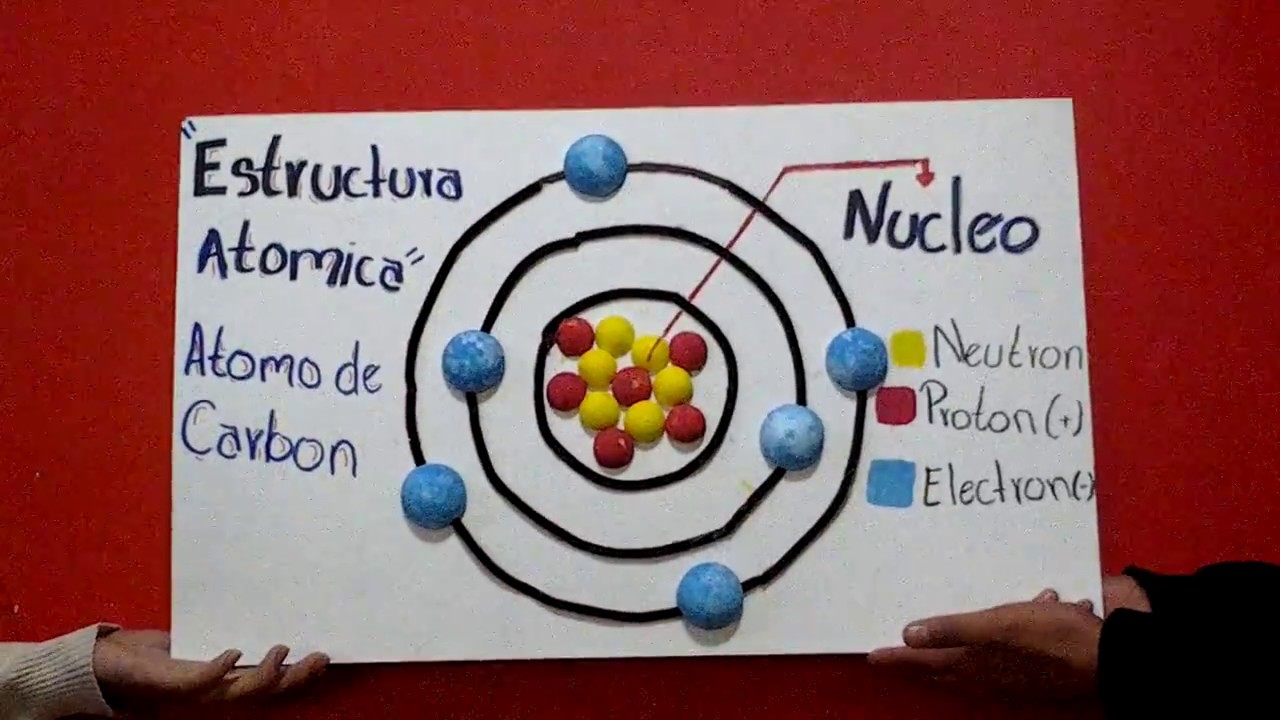
Características. Niveles de energía: Bohr postuló que los electrones en un átomo ocupan niveles de energía discretos y estables, llamados órbitas estacionarias. Órbitas cuantizadas: Las órbitas estacionarias permiten a los electrones girar alrededor del núcleo en trayectorias circulares definidas y cuantizadas. Cuantización del.
Modelo atómico de Bohr. Infografía

Diagrama de Bohr. A partir del modelo de Bohr y los postulados de Bohr, podemos examinar la cuantificación de los niveles de energía de un electrón que orbita alrededor del núcleo del átomo. Suponemos que el electrón tiene una masa mucho menor que la del núcleo y orbita alrededor del núcleo estacionario en movimiento circular obedeciendo la fuerza de Coulomb tal que
Modelo atômico de Bohr quais são os postulados de Bohr para o átomo?
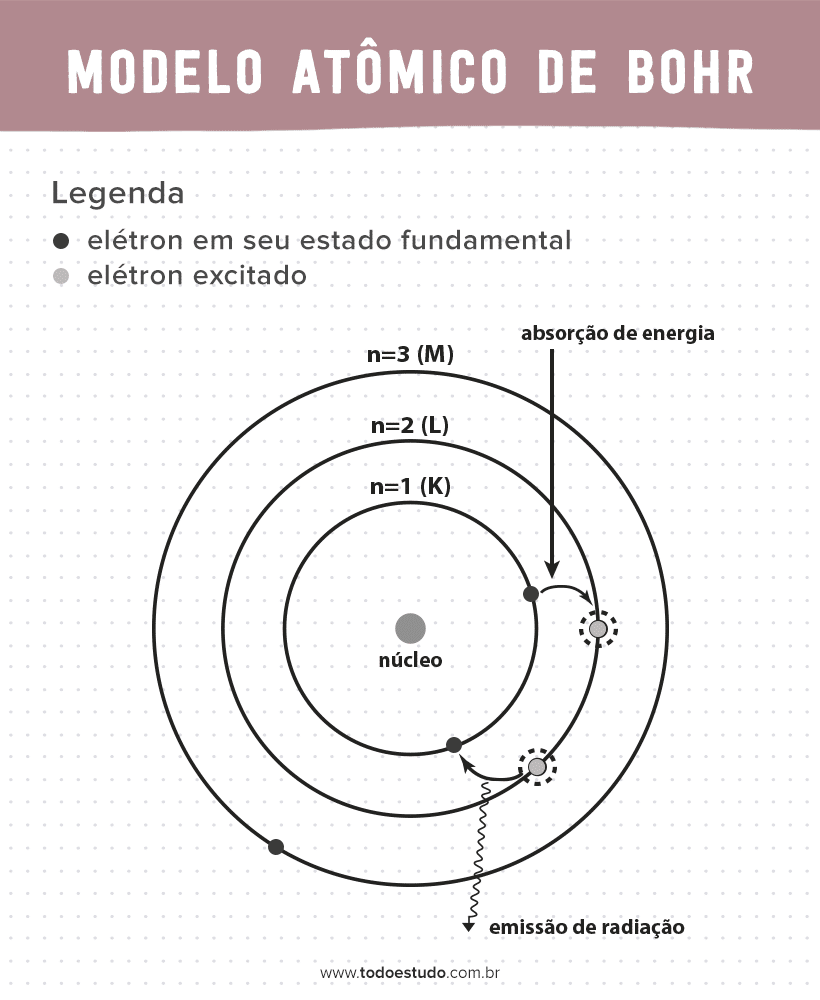
Resumen. Bohr incorporó las ideas de cuantificación de Planck y Einstein en un modelo del átomo de hidrógeno que resolvió la paradoja de la estabilidad atómica y los espectros discretos. El modelo Bohr del átomo de hidrógeno explica la conexión entre la cuantificación de fotones y la emisión cuantificada de átomos.
Niels Bohr Penemu Model Atom Bohr & Peraih Nobel Fisika
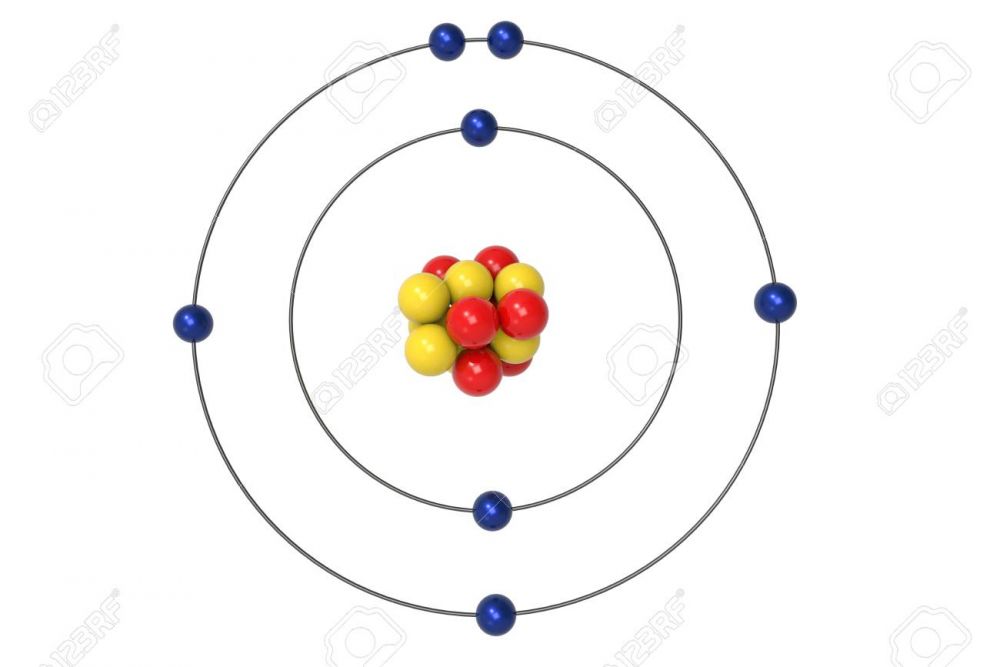
El modelo atómico de Bohr fue creado por Niels Bohr (7 de octubre de 1885 - 18 de noviembre de 1962).También es llamado el modelo atómico Rutherford-Bohr y fue desarrollado en 1913.. Aunque el modelo de Rutherford fue exitoso y revolucionario, tenía algunos conflictos con las leyes de Maxwell y con las leyes de Newton lo que implicaría que todos los átomos fueran inestables.
CHEMISTRY 11 BOHR DIAGRAMS

El modelo atómico de Bohr es la concepción del físico danés Niels Bohr (1885-1962) acerca de la estructura del átomo, publicada en 1913. En el átomo de Bohr, los electrones alrededor del núcleo ocupan únicamente ciertas órbitas permitidas, gracias a una restricción llamada cuantización. Para Bohr, la imagen del átomo como un sistema.
características del modelo atómico de Borh Brainly.lat

El modelo de Bohr es una teoría obsoleta que revolucionó la física en su época. Fue propuesto por Niels Bohr en 1913, y se centró en el átomo de hidrógeno. La teoría postulaba que los electrones en un átomo ocupan orbitales discretos alrededor del núcleo, y que estos orbitales tienen niveles de energía definidos.
El nacimiento de Bohr Y Su Modelo Atomico La fisica y quimica
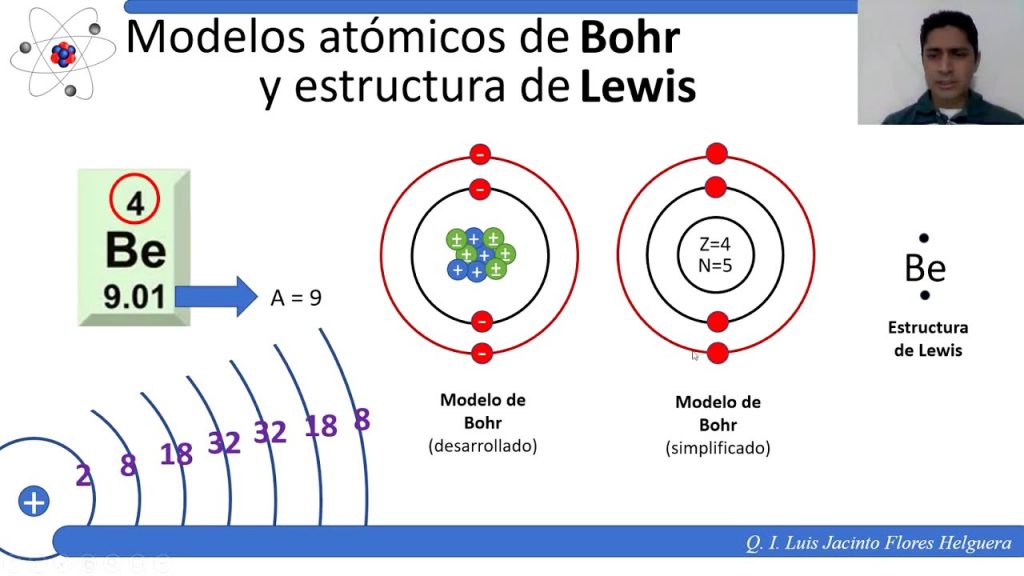
El modelo atómico de Bohr, también conocido como modelo de Rutherford-Bohr, fue una teoría propuesta por el físico danés Niels Bohr en 1913. Esta teoría fue clave para entender la estructura de los átomos, ya que propuso la idea de que los electrones solo pueden existir en ciertas órbitas alrededor del núcleo del átomo.
.
![Modelo Atómico de Bohr [Introducción] Parte 1 YouTube Modelo Atómico de Bohr [Introducción] Parte 1 YouTube](https://i.ytimg.com/vi/g62yjgXDjsg/maxresdefault.jpg)